Vitamina B12: Revisión Completa
Glosario de términos
médicos y bioquímicos al final de la nota.
La vitamina B12 o cobalamina es una vitamina hidrosoluble con la
estructura química más grande y más compleja de todas las vitaminas. Se le
llama cobalamina porque el cobalto forma parte de su estructura química. La
cobalamina pertenece a un grupo de compuestos que contienen cobalto conocidos
como corrinoides, muchos de ellos son biológicamente inactivos en humanos. La
cobalamina puede encontrarse bajo diferentes formas de acuerdo a los grupos
químicos que se le unan, los cuales se unen justamente al átomo de cobalto
(Co), dichos grupos se representan en la figura de abajo con la letra R, y es
así que tenemos entonces la cianocobalamina cuando se une a un grupo cianuro, la
metilcobalamina cuando se une a un grupo metilo, la desoxiadenosilcobalamina si se une a un grupo
desoxiadenosilo e hidroxicobalamina cuando el grupo unido es un grupo hidroxi; la
cianocobalamina se encuentra en cantidades trazas en alimentos y es la forma
más comúnmente utilizada en suplementos de B12. La metilcobalamina y la 5-desoxiadenosilcobalamina
son las únicas formas activas que pueden actuar como cofactores enzimáticos.
Las demás formas mencionadas son transformadas en el organismo en las formas activas.
Consideraciones acerca de su estructura química:
1.- Estructura anular de tipo porfirina con un átomo
de cobalto en el centro.
2.- Cuatro anillos de pirrol reducidos.
3.- Tres tipos de sustituyentes en los anillos de pirrol: metilos,
acetamidos y propionamidos.
4.- Un nucleótido (5,6-dimetil-benzimidazolil)
enlazado al grupo propionamido de uno de los anillos de pirrol.
5.- Un grupo (R) enlazado al átomo de cobalto. Este grupo R
pueden ser radicales cianuro (cianocobalamina), o hidroxilo (hidroxicobalamina),
originándose formas químicamente estables de la vitamina B12 que son
las que se usan en terapéutica; alternativamente R pueden ser sustituyentes metilo
o desoxiadenosilo, formándose las coenzimas activas metilcobalamina
o desoxiadenosilcobalamina respectivamente.
Antes de continuar conviene explicar que es una enzima y que es un
cofactor enzimático. Una enzima es un catalizador biológico, son moléculas proteicas que
aceleran de manera específica reacciones químicas en un ser vivo, sin la
presencia de una determinada enzima, la reacción que ella cataliza no se lleva
a cabo o al menos no se lleva a cabo a la velocidad que un ser vivo necesita
que se produzca para sostener procesos vitales.
Muchas enzimas para funcionar necesitan estar unidas a otra molécula no
proteica que se denomina cofactor, coenzima o grupo prostético. Justamente la
función de muchos minerales y vitaminas es servir como cofactores de
determinadas enzimas. La enzima unida a su cofactor y que por lo tanto es activa,
se denomina holoenzima, mientras que a la parte proteica sin cofactor se le
denomina apoenzima. La apoenzima no tiene actividad catalítica, por lo tanto,
cuando la alimentación no aporta una determinada vitamina sucederá que una o
más enzimas que dependan de esa vitamina como cofactor no funcionarán, lo cual
alterará una o varias vías metabólicas y esto conduce al establecimiento de una
enfermedad por carencia de esa vitamina.
Funciones biológicas
La vitamina
B12 actúa en la síntesis del aminoácido metionina en una reacción que al mismo
tiempo activa el folato (vitamina B 9) el cual es necesario para la transformación
de uridina en timidina, paso clave en la síntesis de ADN. También es necesaria
para la síntesis de mielina, sustancia que envuelve muchas fibras nerviosas y que
es de gran importancia en la transmisión del impulso nervioso y por lo tanto la
B 12 actúa en el mantenimiento y la reparación de los axones neuronales, es
necesaria también en la obtención de energía mitocondrial y en la eritropoyesis
(formación de glóbulos rojos) en la médula ósea. Para realizar estas acciones,
la vitamina B12 actúa como cofactor enzimático de 2 enzimas, la metionina
sintasa y la L-metil-malonil-CoA mutasa.
La metionina
sintasa requiere de meticobalamina para actuar y el paso bioquímico en el cual
interviene es la conversión de metiltetrahidrofolato a tetrahidrofolato, la
cual es una forma activa del folato (que también es una vitamina, habitualmente
mencionada como ácido fólico o vitamina B9) que, como ya dije, interviene en la
síntesis de ADN. En la misma reacción que el metiltetrahidrofolato se
transforma en tetrahidrofolato, la metionina sintasa transforma la homocisteína
en el aminoácido metionina (Figura 1). Esta reacción es muy importante porque
los niveles altos de homocisteína plasmática se correlacionan con mayor riesgo
de efectos cardiovasculares adversos y por otro lado porque la metionina,
previa transformación en S-adenosil metionina, interviene en muchas reacciones
de metilación (también llamadas de donación de metilo), que son de gran
importancia, entre ellas la metilación del ADN.
La donación de metilos es un proceso en el cual se transfiere un pequeño
grupo químico denominado grupo metilo de una molécula a otra para obtener
sustancias con importantes funciones metabólicas. La metilación del ADN cumple
un papel importante en la regulación de la expresión de genes.
La otra
enzima dependiente de B-12, la L-metil-malonil-CoA mutasa, utiliza
5-desoxiadenosilcobalamina como cofactor y convierte el metilmalonil CoA a a
succinil CoA (Figura 2), una molécula implicada en el metabolismo energético
(es un intermediario en el ciclo del ácido cítrico o ciclo de Krebs) y que
también participa en la síntesis del grupo hemo que forma parte de la
hemoglobina. La enzima está implicada en el catabolismo (degradación) de diversos compuestos orgánicos incluyendo
aminoácidos de cadena ramificada (BCAA) y ácidos grasos de cadena impar.
Absorción
La
absorción de la vitamina B12 de los alimentos es un proceso complejo
que requiere una función normal del estómago, el páncreas y el intestino
delgado. El ácido gástrico y la pepsina estomacal liberan la vitamina B12
de los alimentos, permitiéndole unirse a la proteína transcobalamina-1 o haptocorrina, producida
por las glándulas salivales y esofágicas. La haptocorrina protegería a la B12
de su degradación en el medio ácido estomacal. A su vez, las células parietales
gástricas secretan una proteína denominada factor intrínseco (IF) la cual no
puede interactuar con el complejo de vitamina B12-haptocorrina hasta que la
comida pasa al duodeno. En el medio alcalino del intestino delgado, el complejo
B12-transcobalamina-1 es degradado por la tripsina y otras enzimas
pancreáticas, liberando la vitamina B12 para unirse al factor intrínseco
(FI). Los receptores de los enterocitos en la superficie mucosa del íleon
(parte final del intestino delgado), llamados receptores cubam absorben el
complejo IF-B12 solo en la presencia de calcio, el cual es
suministrado por el páncreas. La vitamina B12 puede ser también
absorbida por difusión pasiva, sin participación del FI, pero este proceso es
bastante ineficiente, solo aproximadamente un 1% de la dosis de la vitamina B12
es absorbida pasivamente. Una vez que la vitamina B12 llega a la circulación, se une fácilmente a la
proteína de transporte transcobalamina II. Primero pasa por el hígado que
almacena entre 1000 a 3000 mcg y luego se distribuye en el resto de los
tejidos. La vitamina B12 en el suero se encuentra unida a las proteínas
transcobalamina II y haptocorrina. El complejo formado por la vitamina B12 y la
transcobalamina II se denomina holotranscobalamina y el formado por la B12 y la
haptocorrina se llama holohaptocorrina. La holotranscobalamina contiene
aproximadamente entre el 20 al 30% de la vitamina B12 circulante y representa
la vitamina B12 biológicamente activa, la cual es transportada a todas las
células e ingresa a través de un receptor específico, el CD320. Luego que el
complejo de vitamina B12-transcobalamina ingresa a las células se produce la
degradación lisosómica de la transcobalamina y así la vitamina B12 libre queda
disponible para el metabolismo celular.
Deficiencia:
En
adultos sanos, la deficiencia severa de la vitamina B12 no es común,
principalmente porque el suministro total del cuerpo puede exceder 2,500 μg, el
desgaste diario es lento, y la ingesta dietaría de solo 2.4 μg/día es
suficiente para mantener un nivel adecuado de vitamina B12. Sin
embargo, a nivel mundial, la deficiencia moderada de vitamina B12 es bastante
común, especialmente en las naciones en vías de desarrollo en las que las
personas tienen una baja o limitada ingesta de productos de origen animal (que
son prácticamente la única fuente de la vitamina). En estos países la
deficiencia de B12 se considera la segunda causa de anemia carencial, después
de la anemia por deficiencia de hierro. Según datos de la 1era. Encuesta
Nacional de Nutrición y Salud (2007), el 4.7% de los infantes tuvo una ingesta
de B12 por debajo del requerimiento medio estimado, que se elevó al
25.6 % en las mujeres embarazadas. En individuos de mayor edad, la deficiencia
de vitamina B12 es más común principalmente debido a una absorción
intestinal alterada que puede resultar de una deficiencia marginal a una
deficiencia severa de la vitamina B12 en esta población.
La deficiencia de vitamina B12 conducirá
finalmente a una anemia macrocítica (se llaman así a las anemias que se
caracterizan por un tamaño de los glóbulos rojos superior al normal),
neuropatía periférica y desmejoramiento cognitivo, aunque no necesariamente
siempre se manifiesten estos síntomas (por ejemplo, alrededor del 40% de las
personas mayores con deficiencia de B12 no desarrollan anemia). Las principales
condiciones asociadas a la deficiencia de B12 son: desmejoras en la absorción
(resección quirúrgica, anemia perniciosa autoinmune, pancreatitis crónica,
enfermedad celíaca y de Crohn), y problemas en la digestión gástrica (gastritis
atrófica, aclorhidria, gastrectomía) lo cual disminuye la capacidad de disociar
la vitamina B12 que pueda estar unida a otras sustancias en productos cárnicos.
La
gastritis atrófica autoinmune crónica es un proceso autoinmune dirigido
específicamente a las células parietales gástricas, al factor intrínseco o a
ambos y desemboca en la enfermedad conocida como anemia perniciosa. El daño
celular parietal conduce a la menor producción de ácido gástrico y de factor
intrínseco, acompañado de un aumento compensatorio de los niveles séricos de
gastrina. Se
cree que afecta del 10% al 30% de las personas mayores de 60 años de edad.
Se ha estimado que la anemia perniciosa se encuentra presente en
aproximadamente 2% de los individuos mayores de 60 años de edad. Aunque la
anemia es con frecuencia un síntoma, la enfermedad es de hecho la etapa final de
la gastritis atrófica autoinmune, que resulta en la destrucción de las células
del estómago por anticuerpos propios (autoanticuerpos). La destrucción
progresiva de las células que recubren el estómago provoca una disminución en
la secreción del ácido y las enzimas requeridas para liberar la vitamina B12
ligada a los alimentos. Los anticuerpos contra el FI se unen al FI evitando la
formación del complejo FI-B12, inhibiendo además la absorción de la
vitamina B12. Alrededor del 20% de los familiares de los pacientes
con anemia perniciosa también padecen la misma condición, sugiriendo una
predisposición genética. También se piensa que la infección por Helicobacter
pylori podría estar involucrada en la iniciación de la respuesta autoinmune
en un subconjunto de individuos. Generalmente el tratamiento de la anemia
perniciosa requiere de inyecciones de vitamina B12 para evitar depender
de la absorción intestinal. La suplementación oral en dosis elevadas es otra
opción del tratamiento, porque al consumir 1.000 μg (1 mg)/día de vitamina B12
oralmente debería resultar en la absorción de cerca de 10 μg/día (1% de la
dosis) por difusión pasiva, que como ya vimos es un proceso independiente de la
unión de la vitamina con el factor intrínseco. De hecho, la terapia oral en
dosis elevadas es considerada tan efectiva como la inyección intramuscular.
Los problemas de absorción aumentan a medida
que se envejece y eso hace que la deficiencia de vitamina B12 sea bastante
común en adultos mayores. De acuerdo a datos de estudios europeos el porcentaje
de la población con concentraciones séricas sub óptimas de B12 (menos de 200
pg/ml) es de un 23% en el rango de edad que va de los 19 a los 64 años y
aumenta a un 62% en los mayores de 65 años. Es importante decir que hay estudios
que estiman que el porcentaje de adultos mayores que tienen deficiencia de B12
es bastante menor, pero lo que sí sabemos con certeza que con el envejecimiento
aumenta el riesgo de padecerla.
La malabsorción de vitamina B12
ligada a los alimentos se define como un deterioro en la capacidad de absorber
la vitamina B12 ligada a los alimentos o a las proteínas, individuos
con esta condición pueden absorber la forma libre completamente, ya que
producen factor intrínseco. Mientras la condición es la mayor causa de un
estado pobre de la vitamina B12 en la población de edad avanzada, es
usualmente asociada con la gastritis atrófica y el consecuente descenso de la
producción de ácido estomacal. Debido a que el ácido estomacal es requerido
para la liberación de la vitamina B12 desde las proteínas en los
alimentos, la absorción de la vitamina B12 disminuye. La disminución
de la producción de ácido estomacal también provee de un ambiente propicio para
el sobrecrecimiento estomacal de bacterias anaeróbicas, las que además también interfieren
con la absorción de la vitamina B12. Debido a que la vitamina B12
en los suplementos no está unida a las proteínas, y debido a que el FI se
encuentra aún disponible, la absorción de la vitamina B12
suplementaria no se reduce como en la anemia perniciosa. Así, individuos con
una malabsorción de la vitamina B12 ligada a los alimentos no poseen
un requerimiento mayor de vitamina B12; sólo la necesitan en su
forma cristalina, la que se encuentra en alimentos fortificados y en suplementos
alimenticios.
Otras causas de la deficiencia
de vitamina B12 incluyen la extracción quirúrgica del estómago o de
porciones del intestino delgado donde se localizan los receptores cuban para el
complejo FI-B12. Las condiciones que afectan al intestino delgado,
como los síndromes de mala absorción (enfermedad celíaca y esprúe tropical),
pueden resultar también en una deficiencia de vitamina B12. Debido a
que el páncreas provee tanto las enzimas fundamentales como el calcio necesario
para la absorción de la vitamina B12, la insuficiencia pancreática
puede contribuir a la deficiencia de vitamina B12. Ya que la
vitamina B12 sólo se encuentra en alimentos de origen animal, una
dieta vegetariana estricta ha resultado en casos de deficiencia de vitamina B12.
También los alcohólicos pueden experimentar una absorción intestinal de
vitamina B12 reducida, e individuos con síndrome de
inmunodeficiencia adquirida (SIDA) parecen estar en un mayor riesgo de
deficiencia, posiblemente relacionada a una falla del receptor FI-B12
para captar el complejo FI-B12. Además, el uso a largo plazo de fármacos
como la colestiramina, medicamentos antiácidos, especialmente los inhibidores
de la bomba de protones como el omeprazol entre otros, y de hipoglucemiantes
orales para el tratamiento de la diabetes (metformina) también se han implicado
en la deficiencia de vitamina B12.
Aunque si bien son raros se han
reportado casos de errores innatos del metabolismo de la vitamina B12.
El síndrome de Imerslund-Gräsbeck es un síndrome de malabsorción hereditario de
la vitamina B12 que causa anemia megaloblástica y desórdenes neurológicos
de gravedad variable en sujetos afectados. Síntomas clínicos similares son
encontrados en individuos con una deficiencia hereditaria del FI (también llamada
anemia perniciosa congénita) en los cuales la deficiencia del FI resulta en una
deficiente absorción de la vitamina B12. También se han identificado
mutaciones que afectan el transporte de la vitamina B12 en el organismo.
Más allá de
las complicaciones en la absorción, las deficiencias de B12 son más prevalentes
en poblaciones vegetarianas que en poblaciones omnívoras debido a que la B12 se
encuentra en productos animales. Fuera de los alimentos de origen animal se
encuentra vitamina B12 en la clase de algas Chlorella, en una concentración que
en principio, ingiriendo el polvo desecado en una cantidad adecuada, podría ser
suficiente para prevenir la deficiencia en personas sanas, pero no para tratar
una deficiencia ya establecida.
La
deficiencia congénita y las alteraciones genéticas de la transcobalamina
conducen a deficiencia de vitamina B12 poco después del nacimiento y se
manifiestan clínicamente con manifestaciones hematológicas, neurológicas y
metabólicas propias de la deficiencia de B12, las cuales requieren tratamiento
agresivo incluso cuando el valor sérico de la vitamina B12 se encuentra normal.
Prevalencia
Según la OMS, en 2005, el déficit de B12, definido como dosaje de B12 menor a
148 pmol/l, era cercano al 50% en países como India, y entre el 5 y 30% en el
resto del mundo. En población de riesgo, como las embarazadas y niños, la
prevalencia de déficit de B12 es aún mayor. En una revisión que incluyó 11.381
embarazadas, se evidenció una prevalencia del 27,5% de deficiencia y un 60% de
insuficiencia. En esa misma revisión se evaluaron 22.331 niños, de los cuales
el 12,5% presentaba deficiencia y el 29% insuficiencia para valores menores a
148 pmol/L y 220 pmol/L respectivamente.
A nivel nacional, en 2005, se realizó la primera Encuesta Nacional de Nutrición
y Salud (ENNyS 1). Según los resultados, se estimó que el 4,7% de los menores
de 23 meses y el 3,4% de los niños entre 2 y 5 años tenían una ingesta de B12
por debajo del requerimiento diario. En el grupo de mujeres de 10 a 49 años se
observó que el 3,4% presentaba dosaje de B12 inferiores a 150 pmol/l y el 11,9%
inferiores a 200 pmol/l. En el grupo de embarazadas, el 18,2% presentaba
déficit y el 30,9% insuficiencia. Los datos de nuestro país evidencian una alta
prevalencia de déficit de B12 en la población general, a pesar de presentar una
dieta omnívora, especialmente en los grupos de riesgo, como los niños y las
embarazadas, con una fuerte asociación con la pobreza. No hay estudios
transversales realizados posteriores al ENNyS 1, donde se haya medido el
déficit de B12 en Argentina, sin embargo, no existen indicios socioeconómicos
que evidencien que esta situación haya mejorado. Por el contario, según datos
del Instituto Nacional de Estadística y Censos, INDEC), el porcentaje de personas
que vive bajo la línea de pobreza pasó del 23,4% en 2007 al 42% en 2020, y en
consecuencia, disminuyó el consumo de alimentos de origen animal lo que
ocasionó innumerables compromisos nutricionales como la obesidad, la
desnutrición y los déficits vitamínicos, entre ellos, de la B12.
Los niños y
adolescentes tienen mayor riesgo de déficit por el aumento de los
requerimientos secundarios al crecimiento acelerado, así como también las
embarazadas. Los niños nacidos de madres que tenían depósitos de B12 normales,
nacen con aproximadamente 25 µg de B12 como reserva corporal. Los mismos son
suficientes para que el neonato mantenga valores normales hasta los 3-6 meses
de vida. Es por ello que la lactancia materna exclusiva prolongada es otro
factor de riesgo.
En Argentina la causa más común de déficit de B12 en niños es el aporte
insuficiente, ya sea por dieta deficitaria o por ser hijos de madres con
déficit de B12.
Síntomas y signos de la deficiencia de
vitamina B12
La deficiencia de la vitamina B12 resulta en un deterioro de
las actividades de las enzimas que requieren de la vitamina B12. La
actividad deteriorada de la metionina sintasa resulta en niveles elevados de homocisteina,
mientras que la actividad deteriorada de L-metilmalonil-CoA mutasa resulta en
niveles aumentados de un metabolito del metilmalonil-CoA denominado ácido
metilmalónico (AMM). Los individuos con una leve deficiencia de vitamina B12
pueden no experimentar síntomas, aunque los niveles sanguíneos de homocisteína
y/o AMM podrían estar elevados.
Los síntomas de deficiencia pueden ir de leves a severos e incluso a veces pueden no manifestarse.
Se sugiere que dado que puede llevar un
tiempo relativamente largo que las reservas de B12 se agoten podría deberse a
esto que los síntomas pueden tardar en verse, pero una vez agotadas las
reservas, los síntomas, algunos de los cuales son irreversibles, pueden
manifestarse rápidamente. La deficiencia de vitamina B12 provoca
manifestaciones hematológicas y neuropsiquiátricas que pueden ocurrir juntas
o de manera independientes. La anemia megaloblástica por deficiencia de
folato y otras causas comparten las mismas manifestaciones hematológicas que la
deficiencia de vitamina B12, pero sin las características neurológicas.
Anemia megaloblástica: La actividad disminuida de la metionina sintasa en la deficiencia de
vitamina B12 inhibe la regeneración del tetrahidrofolato (THF) y
atrapa el folato en una forma que no es utilizable por el cuerpo (Figura 3),
resultando en síntomas de deficiencia de folato incluso en presencia de niveles
de folato adecuados. El folato es una vitamina que interviene en el metabolismo
de los precursores de los ácidos nucleicos y de varios aminoácidos. De esta
manera, tanto en la deficiencia de folato como en la de vitamina B12,
el folato no está disponible para participar en la síntesis de ADN. Este
deterioro de la síntesis de ADN afecta a las células de división rápida de la
médula ósea antes que a otras células, resultando en la producción de
eritrocitos grandes, inmaduros, y con poca hemoglobina. La anemia resultante es
conocida como anemia megaloblástica. La suplementación con ácido fólico
proveerá suficiente folato utilizable como para restaurar la formación normal
de glóbulos rojos. Sin embargo, si la causa es la deficiencia de vitamina B12,
esta persistirá a pesar de la resolución de la anemia. Así, la anemia
megaloblástica no debería tratarse con ácido fólico hasta que la causa
subyacente haya sido determinada. Los síntomas secundarios a la anemia son: fatiga, disnea y poca
tolerancia al ejercicio. Además de la anemia macrocítica, puede observarse
aplasia medular y pancitopenia; menos frecuentemente se han descripto casos de
pseudo microangiopatía trombótica, con síntomas similares al síndrome urémico
hemolítico.
Síntomas neurológicos: Los síntomas
neurológicos de la deficiencia de vitamina B12 incluyen
entumecimiento y cosquilleo de las manos y, más comúnmente, en los pies
(parestesias bilaterales); hipotonía, hiperreflexia, parálisis, dificultad para
caminar (alteraciones de la marcha y del equilibrio), disminución de la
sensibilidad vibratoria y posicional, pérdida de la visión, las manifestaciones
psiquiátricas son pérdida de memoria, desorientación, delirio, demencia, depresión,
manía y alucinaciones. Existen además reportes que asocian al déficit de B12 como una
causa de epilepsia.
Aunque, la progresión de las complicaciones neurológicas
generalmente es gradual, dichos síntomas no son reversibles con el tratamiento
de la deficiencia de vitamina B12, especialmente si han estado
presentes por mucho tiempo. Aunque los síntomas neuropsiquiátricos suelen desarrollarse
después de las anormalidades hematológicas, las complicaciones neurológicas no siempre
están asociadas con la anemia megaloblástica y son el único síntoma clínico de
la deficiencia de vitamina B12 en alrededor de un 25% de los casos, teniendo en estos casos los
pacientes un hematocrito normal o
un volumen corpuscular medio (VCM) normal.
La metionina es
precursora de la S-Adenosilmetionina (SAM), molécula necesaria para el
mantenimiento de la mielina. Es por ello que, ante el déficit de B12, se genera
desmielinización y polineuropatía periférica. Aunque se sabe que la deficiencia de
vitamina B12 daña la vaina de mielina que cubre los nervios
craneales, los nervios espinales y los nervios periféricos, y que puede causar
degeneración subaguda combinada de las columnas dorsal y lateral de la médula
espinal, los
procesos bioquímicos que conducen al daño neurológico en la deficiencia de
vitamina B12 aún no son bien comprendidos. La SAM también está
implicada en la formación de creatina, fuente de reserva energética muscular, y
es la responsable de los movimientos mioclónicos que aparecen en pacientes con
déficit de B12
Aún
no está claro por qué ciertos pacientes son propensos a las complicaciones
hematológicas y otros tienen secuelas neurológicas, pero aquellos con
anormalidades subyacentes como enfermedades neurológicas preexistentes o
condiciones de falla de la médula ósea pueden ser más propensos a desarrollar
efectos secundarios relacionados con esas condiciones.
Síntomas
gastrointestinales: El dolor en la lengua, la pérdida de apetito (anorexia) y la
constipación también han sido asociados a la deficiencia de vitamina B12.
El origen de estos síntomas no está claro, pero puede estar relacionado con la
inflamación del estómago subyacente a algunos casos de deficiencia de vitamina
B12, y a la progresiva destrucción del revestimiento estomacal. En la
deficiencia de vitamina B12, la glositis atrófica (inflamación de la lengua con
daño en las papilas) es una enfermedad común, aunque inespecífica.
Otros hallazgos: En la deficiencia de vitamina B12 y folato
se observa mayor riesgo de trombosis, posiblemente como resultado de la
hiperhomocisteinemia. En un ensayo clínico en Nigeria se observó que el espesor
de la íntima carotídea aumentaba 0,01 mm por cada 1 punto que aumentaba la
homocisteína en pacientes con déficit de B12. En los últimos años, el espectro
de síntomas se ha ampliado y se agregaron: falla del crecimiento, apatía, disfunción
gastrointestinal con vómitos o rechazo de los alimentos sólidos, dificultades
en la succión, malabsorción, infertilidad e hiperpigmentación cutánea. Asimismo se relacionó el déficit de B12 con abortos espontáneos,
nacimientos pretérmino, bajo peso al nacer y retardo en el crecimiento
intrauterino. Hay estudios que muestran que los recién nacidos de madres con
déficit de B12 tienen un riesgo cinco veces mayor de presentar defectos en el
cierre del tubo neural.
Por otro lado, la B12 es importante en la síntesis de catecolaminas. Su
deficiencia produce disfunción autonómica y afecta la regulación simpática de
la presión arterial. En base a esto, es que se sugirió que el déficit de B12 se
relaciona con algunos tipos de síncope y al síndrome de taquicardia ortostática
postural. Menos conocidas son las manifestaciones dermatológicas
del déficit de B12, aunque suelen ser un signo frecuente. La hiperpigmentación
en el dorso de manos y pies, con mayor intensidad en las uniones
interfalángicas, "hiperpigmentación de los nudillos", es la más
reportada.
Síntomas
por deficiencia en la dieta durante la primera infancia y la niñez
Los primeros 2 años
de vida de un niño son críticos para la mielinización de las neuronas, por lo
que para el desarrollo neurológico durante este período se requiere el depósito
adecuado de B12. El hijo de una madre con deficiencia de vitamina B12 puede
haber nacido con deficiencia de B12 o dicha deficiencia puede ocurrir cuando
solo recibe lactancia materna, usualmente entre los 4 y los 6 meses de edad.
Las manifestaciones típicas de la deficiencia de vitamina B12 en los niños son:
mal desarrollo cerebral y mal crecimiento y desarrollo general, regresión del
desarrollo, hipotonía, dificultad en la alimentación, letargo, temblores, hiperirritabilidad
y coma. Las imágenes cerebrales pueden mostrar atrofia y retardo de la
mielinización. Puede haber anemia.
El aporte de vitamina B12 mejora
rápidamente la capacidad de respuesta y muchos niños se recuperan por completo.
Sin embargo, cuanto más prolongado es el período de deficiencia más
probabilidad hay de que las discapacidades sean permanentes. Las madres de los
niños con deficiencia de vitamina B12 suelen tener anemia perniciosa no
diagnosticada, pero pueden tener el antecedente de una cirugía de bypass
gástrico, síndrome del intestino corto o seguir una dieta vegetariana o vegana.
EMBARAZO
La deficiencia de B12 se relaciona
con embarazos de mala evolución, riesgo de parto prematuro, bajo peso al nacer;
defectos del tubo neural y cardiopatía congénita (estas dos últimas asociadas a
déficit de folatos) por consiguiente mayor riesgo de morbilidad infantil.
En una revisión sistemática y en un
meta análisis que incluyó dieciocho
estudios (11.216 observaciones), se evaluaron las asociaciones de las
concentraciones de B12 en plasma materno, con el peso al nacer de la
descendencia y la duración de la gestación. No se observó asociación lineal
entre los niveles maternos de B12 durante el embarazo y el peso al nacer, pero
valores de B12 inferiores a 148 pmol / L se asociaron con mayor riesgo de bajo
peso al nacer. Hubo asociación lineal entre niveles maternos de B12 y parto
prematuro.
Sin embargo, en otra revisión
sistemática y meta análisis, los autores concluyeron que la insuficiencia de
B12 durante el embarazo es común incluso en poblaciones no vegetarianas y que
las concentraciones de B12 disminuyen desde el primer al tercer trimestre pero,
no encontraron asociación consistente entre la insuficiencia de B12 y bajo peso
al nacer.
Síntomas clínicos
de la deficiencia de Vit-B12 – Sumario
• Anemia Megaloblástica
Fatiga
Cansancio
Mareos
• Enfermedad
desmielinizante del sistema nervioso central
Hormigueo o entumecimiento en los dedos de
manos y pies
Problemas de marcha y equilibrio
Irritabilidad, depresión, falta de memoria y
problemas de atención y concentración.
Trastornos psiquiátricos: demencia, manía,
psicosis y cambios de personalidad
Atrofia óptica
• Disfunción
gastrointestinal
Glositis
Malabsorción
• Infertilidad
• Vitiligo
Evaluación
y Diagnóstico
Es
difícil hacer el diagnóstico clínico de la deficiencia de vitamina B12 o
confirmarla por medio de análisis clínicos. La historia clínica puede incluir
los síntomas de la anemia, los trastornos subyacentes que causan la
malabsorción y los síntomas neurológicos. Los síntomas neurológicos más comunes
son las parestesias o insensibilidad simétrica o los trastornos de la marcha.
El examen físico puede revelar palidez, edema, alteraciones de la pigmentación
cutánea, ictericia o defectos neurológicos como la alteración de la
sensibilidad vibratoria, posicional y táctil, la ataxia y la debilidad. Si se
trata de un paciente que lleva una dieta
vegetariana o vegana y no presenta síntomas, confirmar la deficiencia
por métodos de laboratorio también se hace difícil.
• Análisis de la vitamina B12
La primera prueba a realizar para confirmar el diagnóstico de
deficiencia de vitamina B12 es la determinación de su nivel sérico. Para
definir la deficiencia de vitamina B12, en forma convencional se utiliza un
nivel de corte <150 pmol/l, pero los médicos también deben consultar el
rango de referencia proporcionado por el laboratorio local. Según la
Organización Mundial de la Salud (OMS), se define déficit de B12 con valores
inferiores a 148 pmol/l . La Sociedad Argentina de Pediatría (SAP) sugiere
mantener valores mayores a 360 pmol/l. Para el análisis bioquímico de B12 no se
requiere el ayuno. Es una prueba barata, fácil de hacer en atención primaria, y
ampliamente disponible. Aunque un nivel extremadamente bajo (<100 pg/ml)
comúnmente se asocia con manifestaciones clínicas, su observación es poco
frecuente. Si como puntos de corte para el diagnóstico de deficiencia de
vitamina B12 se utilizan los valores de referencia más bajos dados por el
laboratorio es común hallar valores negativos y positivos falsos (hasta en el
50% de los análisis).
La
elevada tasa de resultados negativos
y positivos falsos puede deberse al hecho de que solo el 20% de
la vitamina total medida es liberada de la proteína celular, la
transcobalamina; el resto se une a la haptocorrina, una proteína de función
desconocida.
La
vitamina B12 unida a haptocorrina, a pesar que representa alrededor del 80% de
la vitamina B12 circulante, se considera metabólicamente inerte. La
holotranscobalamina se ha señalado como uno de los primeros marcadores de la
deficiencia de B12, con un mejor desempeño para detectar la deficiencia que la
medición sérica de vitamina B12 total, cuyos niveles corresponden principalmente
a la vitamina unida a haptocorrina.
Para
descartar el diagnóstico de deficiencia de vitamina B12 en los pacientes con
anormalidades clínicas compatibles y dadas las limitaciones que poseen los
análisis disponibles, los médicos NO
deben usar los límites inferiores del rango normal referido por los
laboratorios.
• Hemograma completo con hemoglobina, volumen corpuscular
medio (VCM), hematocrito y frotis sanguíneo
La presencia de anemia, particularmente si es
macrocítica (VCM >100 fL), aumenta la sospecha de deficiencia de B12 y
requiere una prueba rápida de B12 y de los niveles de folato.
Una causa de anemia macrocítica es la
megaloblastosis, referida a la división celular retardada causada por un
bloqueo en la síntesis de ADN. Esto ocurre exclusivamente en la deficiencia de
B12 o de folato.
Otros hallazgos hematológicos en la deficiencia de
B12 son: leucopenia leve, trombocitopenia, pancitopenia y neutrófilos
hipersegmentados.
Es importante recordar que el VCM puede ser normal
en presencia de microcitosis concomitante, como sucede en la deficiencia de
hierro o la talasemia. Si está clínicamente indicado, deben hacerse pruebas de
detección para estas condiciones.
Las guías del Reino Unido recomiendan que antes de
comenzar el tratamiento se controle el nivel del vitamina B12 total en el
suero, pero en entornos de escasos recursos, donde las pruebas de B12 y folato
no están fácilmente disponibles o son caras, los médicos pueden iniciar el
tratamiento ante el hallazgo de una anemia macrocítica (u otros signos
objetivos de deficiencia de B12).
Cuando no se cuenta con los valores de laboratorio
de B12 o folato, ese enfoque puede ser más seguro que el de no tratar. De modo
que debe administrarse B12 y ácido fólico juntos y reevaluar después de 1
semana mediante un nuevo hemograma completo.
• Folato en
suero
Para que el folato cumpla
con su función celular debe actuar sinérgicamente con la vitamina B12, de modo
que debe ser revisado y corregido si fuera necesario. Las deficiencias de B12 y
folato pueden coexistir, particularmente en situaciones de malabsorción o
deficiencia nutricional severa.
Estudios
especializados
Pruebas para determinar la causa de
la deficiencia de vitamina B12
Sospecha de anemia perniciosa
La prevalencia de anemia
perniciosa es de aproximadamente 4% en países europeos y aumenta con la edad.
Es una forma de gastritis atrófica con destrucción autoinmune de las células
parietales del estómago, con la pérdida de la producción de factor intrínseco,
lo que conduce a la reducción de la absorción de B12.
Hay una asociación con
otras condiciones autoinmunes, aunque pueden ocurrir en forma aislada. Algunos
investigadores sugieren que los estudios para la anemia perniciosa deben
considerarse en los pacientes con manifestaciones clínicas de deficiencia de
B12 (síntomas hematológicos o neurológicos) independientemente de los niveles
de B12, también como en aquellos con niveles bajos de B12 en suero sin ninguna
causa o factores de riesgo obvios.
Los estudios para la
anemia perniciosa son:
• Análisis de anticuerpos
contra el factor intrínseco
Son
altamente específicos de la anemia perniciosa (95-100%), lo que significa que
los positivos falsos ocurren el en el 5% de los casos. Sin embargo, la
sensibilidad de este test es solo del 50-60%, de manera que un resultado
negativo no descarta la enfermedad.
• Condiciones de malabsorción
Estudiar a
los pacientes en quienes se sospecha malabsorción gastrointestinal y considerar
su derivación al gastroenterólogo. Si el paciente consume suficiente cantidad
de vitamina B12 y la deficiencia está confirmada, entonces existe malabsorción.
Un análisis positivo de anticuerpos antifactor intrínseco o anticélulas
parietales indica anemia perniciosa. Si se halla un nivel elevado de gastrina
sérica en ayunas y un nivel bajo de pepsinógeno I sérico se puede hacer el
diagnóstico de gastritis atrófica crónica. Algunos especialistas recomiendan
hacer una endoscopia para confirmar la gastritis y descartar el tumor
carcinoide gástrico y otros cánceres del estómago, dado que los pacientes con
anemia perniciosa tienen mayor riesgo de desarrollar esas neoplasias.
• Otras investigaciones
especializadas
• Holotranscobalamina
Es la forma
funcional de la vitamina B12 absorbida y utilizada por los tejidos.
Generalmente se correlaciona bien con niveles totales de B12, medido por los
ensayos de B12 estándar. La ventaja de medir esta forma de B12 es que da una
indicación de la B12 biológicamente activa en el cuerpo y no se ve afectada por
condiciones que disminuyen la proteína de unión a B12, la haptocorrina,
como el embarazo, el uso de anticonceptivos orales y la infección por VIH.
Recientemente el National
Institute for Health and Care Excellence (NICE) del Reino Unido de Gran Bretaña
ha aprobado un ensayo para la holotranscobalamina sugiriendo que podría
reemplazar a la prueba B12 total, particularmente en situaciones de resultados
de B12 indeterminados o limítrofes.
Una concentración de holotranscobalamina sérica
entre 40 y 100 pmol/l podría ser el objetivo para definir B12 suficiente en adultos.
La SAP recomienda valores mayores a 45 pmol/l.
Por otro lado, la espectrometría de masa realizada en el screening neonatal
ampliado detecta la deficiencia de B12 a través del incremento de la
propionilcarnitina (C3), que aumenta por el exceso de propionil Coa, secundario
al déficit de B12. Aunque, según la causa, la propionilcarnitina podría no
estar elevada al momento del nacimiento, por lo cual su sensibilidad es baja.
Medición del ácido metilmalónico sérico y la homocisteína total
Estas mediciones son útiles para hacer el diagnóstico de
deficiencia de vitamina B12 en los pacientes que no han recibido tratamiento.
Los niveles del ácido metilmalónico (AMM) sérico y de la homocisteína total están
muy elevados en la gran mayoría (>98%) de los pacientes con deficiencia
clínica de vitamina B12, incluyendo aquellos que solo tienen las
manifestaciones neurológicas (por ej., sin anemia).
El AMM se ha recomendado como una prueba de segunda línea para el diagnóstico
de la deficiencia de B12, aunque su disponibilidad en la práctica clínica a
veces es limitada. Para confirmar la deficiencia de B12, el nivel de AMM, por
sí mismo, tiene una sensibilidad del 86% y >99% si se combina con la
elevación de la homocisteína.
Las
guías sostienen que cuando la probabilidad clínica es elevada pero los
resultados del análisis de B12 en suero de primera línea están en el límite, o
cuando hay discordancia entre los valores de B12 los y síntomas clínicos, las
determinaciones del AMM y de homocisteína son útiles para determinar la
deficiencia bioquímica de la B12.
Los
niveles elevados de AMM sérico y de homocisteína total disminuyen
inmediatamente después del tratamiento y pueden ser medidos para documentar que
el reemplazo de la vitamina B12 es adecuado. Los niveles de estos metabolitos
son normales hasta en el 50% de los pacientes con niveles bajos de vitamina B12
que no muestran respuesta hematológica o neurológica a la terapia de reemplazo,
lo que indica que los valores bajos de B12 son resultados positivos falsos.
En
los pacientes con signos clínicos compatibles o en quienes se desea hacer un
tratamiento empírico utilizando puntos finales definidos para documentar la
respuesta clínica y debido a las limitaciones de los análisis de vitamina B12
para confirmar el diagnóstico de deficiencia, puede ser adecuado medir el AMM
sérico, la homocisteína total o ambos. Un nivel elevado de AMM sérico es
bastante específico de deficiencia de vitamina B12 a la vez que siempre
disminuye con el tratamiento con vitamina B12.
En la insuficiencia renal se observa un ligero aumento AMM (300
a 700 nmol/l). Sin embargo, casi todos los pacientes con anemia megaloblástica
o mielopatía tienen niveles de AMM >500 nmol/l, y el 86% tiene niveles
>1.000 nmol/l. El nivel de AAM
también puede aumentar en condiciones tales como la deshidratación y el
crecimiento bacteriano excesivo en el intestino delgado, dando lugar a
resultados positivos falsos. El nivel de homocisteína sérica es menos
específico, dado que también se eleva en la homocistinuria clásica, por deficiencia
de folato, de vitamina B2 y B6, en el hipotiroidismo, insuficiencia renal,
hipovolemia, enfermedades neurodegenerativas, patologías malignas y algunos
fármacos (metotrexato, teofilina, fenitoína), de modo que es menos específica
que el AMM para el diagnóstico de deficiencia de B12.
Dado que los niveles de homocisteína pueden verse afectados por
el almacenamiento de la muestra a temperatura ambiente, la sangre debe
guardarse en hielo y ser trasladada a un laboratorio para ser procesada dentro de
las 2 horas (siempre que se mantenga en hielo). La falta de rapidez en la
separación del plasma también podrían afectar los niveles de homocisteína y
aumentarlos hasta un 10%.
La
elevación de los niveles de AMM puede ocurrir cuando los niveles de B12 son
< 400 pmol/l, valor que es más elevado que el umbral asociado con resultados
clínicos adversos, y puede estar particularmente asociado con el deterioro
cognitivo acelerado.
La mayoría de los
estudios coincide en que para realizar un diagnóstico de déficit de B12 se
requiere efectuar más de una determinación. Schedvin et al. recomendaron
realizar como primera línea diagnóstica un dosaje de homocisteína y, ante
valores alterados, efectuar una segunda prueba para diferenciar déficit de B12
y de ácido fólico. Herrmann y Obeid propusieron el dosaje de
holotranscobalamina como primera línea diagnóstica, y a los pacientes con
dosajes entre 23 y 75 μmol/l realizarles dosaje de ácido metilmalónico para
confirmar el diagnóstico. En este estudio se demostró que la holotranscobalamina
presentaba mayor sensibilidad y lograba evidenciar el déficit de B12 de forma
más temprana que el dosaje de B12 total.
La Ingesta Diaria Recomendada (IDR)
La IDR (que
se define como el promedio
del nivel de ingesta dietética diaria suficiente de un nutriente como para
cubrir las necesidades de casi todos los individuos sanos en una etapa de la
vida y en un grupo de género específico) para la
vitamina B12 fue revisada por la Junta de Nutrición y Alimentos
(JNA) del Instituto de Medicina de los Estados Unidos en 1998. Debido al
incremento del riesgo de una malabsorción de vitamina B12 ligada a
los alimentos en adultos mayores, la JNA recomendó que los adultos sobre los 50
años de edad obtengan la mayor parte de la IDR de alimentos fortificados o de
suplementos que contengan vitamina B12.
Las sociedades de
nutrición de Alemania, Austria, y Suiza son las editoras de los "D-A-CH
reference values for nutrient intake" (valores de referencia para ingesta
de nutrientes de Alemania, Austria y Suiza), los cuales son revisados
regularmente. Estos valores de referencia fueron actualizados en 2018. La
ingesta estimada para adultos se basa en concentraciones séricas de
holotranscobalamina adecuadas y ácido metilmalónico. Los valores estimados para
niños y adolescentes son extrapolados de los valores de referencia para
adultos, considerando las diferencias en la masa corporal y factores de
crecimiento. Para niños de menos de 4 meses se estableció un valor estimado
basado en la ingesta de vitamina B12 vía la lactancia materna. Los valores de
referencia para mujeres embarazadas y en período de lactancia consideran los
requerimientos del feto y la pérdida a través de la leche materna. Los valores
estimados de ingesta de vitamina B12 para infantes, niños y adolescentes van
desde 0,5 a 4,0 µg / d. Para adultos, el valor estimado se estableció en 4.0 µg
/ d, y para embarazadas y mujeres en etapa de lactancia en 4.5 and 5.5 µg / d,
respectivamente.
|
Ingesta Diaria
Recomendada (IDR) para Vitamina B12 |
|||
|
Etapa de la Vida |
Edad |
Instituto de Medicina (μg/día) |
D-A-CH References Values (μg/día) |
|
Infantes |
0-6 meses |
0.4 (IA) |
0.5 (IA) |
|
Infantes |
6-12 meses |
0.5 (IA) |
1.4 (IA) |
|
Niños |
1-3 años |
0.9 |
1.5 |
|
Niños |
4-7 años |
1.2 |
2.0 |
|
Niños |
7-9 años |
1.2 |
2.5 |
|
Niños |
10-13 años |
1.8 |
3.5 |
|
Adolescentes
|
14-18 años |
2.4 |
4.0 |
|
Adultos |
19-50 años |
2.4 |
4.0 |
|
Adultos |
51 años y más |
2.4* |
2.4* |
|
Embarazo |
Todas las edades |
2.6 |
4.5 |
|
Período
de lactancia |
Todas las edades |
2.8 |
5.5 |
|
·
IA Ingesta adecuada. Establecida por la Junta de Nutrición y
Alimentos del Instituto de Medicina de los EE.UU., la IA es un valor de ingesta recomendada basado en estimaciones
observadas o determinadas experimentalmente de la ingesta de nutrientes por
un grupo de personas sanas, el que se asume como adecuado. Se establece la IA
cuando no se puede determinar la IDR. *
La ingesta de vitamina B12 debiera provenir de
suplementos o de alimentos fortificados debido al incremento de la mala absorción ligada a los
alimentos relacionada con la edad. |
|||
Otra
población con riesgo de déficit de B12 la constituyen las mujeres embarazadas,
ya que se ha demostrado que la concentración de la B12 presenta una disminución
fisiológica del 70-75% alrededor de la semana 20 de embarazo. Teniendo en
cuenta este fenómeno es que se estableció que las embarazadas que comienzan su
embarazo con un dosaje de B12 total menor a 250 pmol/l, presentan mayor riesgo
de déficit y algunos autores recomiendan buscar valores mayores a 300 pmol/l al
comienzo del embarazo para evitar la insuficiencia e indicar suplementación a
las mujeres que presenten valores límites.
Fuentes alimenticias
Sólo las bacterias pueden sintetizar la vitamina B12. La
vitamina B12 está presente en productos animales como la carne, las
aves de corral, el pescado (incluyendo mariscos), y en menor medida, en
productos lácteos y huevos. La leche fresca pasteurizada contiene 0.9 μg por
vaso (250 ml) y es una fuente importante de vitamina B12 para
algunos vegetarianos. El rumen del ganado vacuno, ovino y caprino contiene
cepas bacterianas capaces de sintetizar B12, que luego es absorbida en el
intestino y pasa a los distintos tejidos y a la leche. El cerdo y las aves, por
su condición de omnívoros, obtienen la B12 de su alimentación, por lo que su
contenido en este tipo de carnes suele ser menor que en la vacuna. En el ambiente acuático, la B12 producida por
ciertas bacterias y archaebacterias es captada por el fitoplancton, que es
consumido por el zooplancton y el resto de la cadena alimentaria marina, por lo
cual pescados y mariscos también son fuente de B12. En general el contenido de
vitamina B12 es mayor en los pescados carnívoros grandes que en peces pequeños.
Aquellos vegetarianos estrictos que no comen ningún producto animal (veganos)
necesitan tomar un suplemento de vitamina B12 para satisfacer
sus requerimientos. Pero en general todos los vegetarianos están en riesgo de
sufrir una deficiencia de B12. Análisis recientes revelaron que algunos
alimentos vegetales y algas y hongos comestibles, contienen sustanciales
cantidades de vitamina B12 pero la caracterización de los compuestos
hallados reveló que se trata de corrinoides inactivos en humanos. La mayoría de
las algas azul verdes comestibles (cyanobacteria), entre ellas la espirulina, contienen un
corrinoide inactivo conocido como pseudovitamina B12. Sin embargo en
el alga chlorella se halla vitamina B12 activa. En muchos de estos alimentos
encontramos vitamina B12 activa y corrinoides inactivos y como estos últimos
pueden bloquear la acción de la vitamina B12 activa las microalgas no son una fuente
confiable de B12. Por la misma razón no se consideran adecuados los suplementos
que combinan espirulina con vitamina B12. La Academia Americana de Nutrición y
Dietética en su documento de posición sobre alimentación vegetariana12 indica
que los alimentos fermentados, como el tempeh, algas nori, espirulina, alga
chlorella, o la levadura nutricional no fortificada no pueden ser consideradas
fuentes adecuadas o prácticas para el aporte de B12 para vegetarianos. Los
champignones de la familia Agariscus Bisporus contienen muy bajas
concentraciones de B12 y el Shiitake, unos de los hongos más consumidos en las
dietas vegetarianas, tiene altas concentraciones, pero con gran variabilidad
(5.61 ± 3.9g/100g peso seco) por lo cual no podemos saber con precisión cuanta
B12 estamos incorporando al ingerir estos alimentos. Además,
varios factores afectan la bioactividad de la vitamina B12 en alimentos.
Por ejemplo, la vitamina B12 es parcialmente degradada y pierde su
actividad biológica durante la cocción y el almacenamiento de alimentos.
Las almejas y el bife de hígado vacuno son las
fuentes más ricas de B12, conteniendo alrededor de 93 y 80 μg de B12 en una
porción de 100 gramos. La cantidad de B12 encontrada en 100 g de pollo varía de
alrededor de 4 μg en el hígado entero a 0.04 μg en el cuello del pollo. El
cerdo contiene cada 100 g entre 0.35 μg de B12 en una salchicha a alrededor de
13.4 μg en el hígado. El contenido de
B12 en pescados va desde alrededor de 9 μg en medio filete de salmón rojo a
alrededor de 0.59 μg en 100 gramos de atún aleta amarilla. La leche contiene
entre 0.3 y 0.4 μg/100 g de B12, con una tasa de absorción de alrededor del
65%. Los quesos tienen un contenido de B12 que va del 20 al 60% del contenido
de la leche. Un huevo entero contiene entre 0.9 y 1.4 μg/100 g. La vitamina B12
puede ser destruida por el calor y por esta razón, hervir la leche puede
destruir entre un 30 a un 50% de la B12, dependiendo de la duración del
calentamiento.
La mayoría de las personas no tiene problemas para alcanzar la IDR de
2.4 μg/día de vitamina B12 en la comida. De acuerdo a una encuesta
nacional en los Estados Unidos, la ingesta promedio de vitamina B12
es de alrededor de 5.4 μg/día para hombres adultos, y 3.4 μg/día para mujeres
adultas. Los adultos mayores de 60 años tuvieron una ingesta promedio de 4.8
μg/día. Sin embargo, el consumo de cualquier tipo de dieta vegetariana incrementa significativamente (y a veces de
manera repentina) la prevalencia de la deficiencia de vitamina B12
en individuos de todas las edades. En un estudio publicado en Nutrition Reviews
en febrero del 2013 (Nutrition Reviews, Volume 71, Issue 2, 1 February 2013, Pages 110–117, https://doi.org/10.1111/nure.12001
How
prevalent is vitamin B12 deficiency among vegetarians? se intentó establecer la tasa de
depleción y deficiencia entre vegetarianos y veganos. Aunque alguna vez se
pensó que la deficiencia de B12 era extremadamente rara excepto entre
vegetarianos estrictos (veganos), ahora sabemos que dicha deficiencia es
relativamente común entre las personas que llevan cualquier tipo de dieta
vegetariana, incluyendo la dieta lacto-ovo-vegetariana. Para realizar este
trabajo se analizaron diversos estudios que reportaron el estado de la B12 a
partir de medidas de holo-transcobalamina II (holo-TCII) y/o ácido
metilmalónico (AMM) sérico o urinario. Aunque como ya hemos visto existen
diversas técnicas para medir el estado de la B12, por ejemplo medir la
concentración de la vitamina en plasma o suero, medir el volumen corpuscular
medio (VCM) de los eritrocitos o la concentración de homocisteína, los estudios
más recientes indican que la medición de holo-TCII y AMM son los indicadores
más precisos del estado de la B12 mientras que la medida de B12 plasmática o
sérica y el VCM son pocos confiables. Se ha sugerido que la progresión desde un
estado normal de B12 a la deficiencia pasa a través de un estado llamado depleción y que la holo-TCII es el
mejor marcador en este estado mientras que el MMA es el mejor marcador del
estado de la B12 cuando los depósitos están exhaustos y se ha llegado a la deficiencia.
También se sugiere que se debería usar más de una técnica de evaluación para
determinar el estado de la B12 y que los investigadores que reportaron el
estado de la B12 entre vegetarianos basados en el uso del nivel de B12 sérica
como un marcador del estado de la B12 probablemente subestimaron la tasa de
deficiencia debido a la imprecisión inherente a este método de evaluación. Según
el criterio utilizado para definir deficiencia, la prevalencia de la misma en
vegetarianos puede ir desde el 11% al 90% de la población
Uno de los principales hallazgos es que los vegetarianos
desarrollan deficiencia de B12 independientemente de las características demográficas,
el lugar de residencia, la edad, o el tipo de dieta vegetariana consumida.
En niños se reportaron tasas más altas de deficiencia entre
aquellos que siguieron un estilo de vida vegetariano desde el nacimiento,
comparado con aquellos que lo adoptaron en una etapa posterior de la vida. Este
hallazgo es probablemente debido a que las madres de estos niños son también
vegetarianas y sus depósitos de B12 son bajos lo que da como resultado bajos
depósitos de B12 en su descendencia.
Otro hallazgo sorprendente fue que la tasa de deficiencia fue
mayor entre veganos que usaron suplementos de B12 (88%) que entre aquellos que
no los usaron (83%). Este hecho puede deberse a dos factores: 1) Uso de los
suplementos con una frecuencia menor a la necesaria 2) Uso de los suplementos con
una dosis menor que la necesaria para mantener un estado de B12 adecuado. Si
bien los suplementos orales han demostrado ser efectivos para corregir la
deficiencia de B12, la dosis de B12 debería ser al menos de alrededor de 100 veces
más alta que la IDR para evitar una deficiencia. En casos de deficiencia ya
establecida, puede ser necesario ingerir una dosis de al menos 200 veces mayor
que la IDR para alcanzar los resultados más deseables.
Algunos alimentos con cantidades substanciales de vitamina B12
son listados en la tabla a continuación con su contenido de vitamina B12
en microgramos (μg).
|
Alimento |
Porción |
Vitamina B12 (μg) |
|
Almejas (al vapor) |
100 gramos |
98.9 |
|
Mejillones (al vapor) |
100 gramos |
24.0 |
|
Caballa (cocida, al horno) |
100 gramos |
18.9 |
|
Cangrejo (al vapor) |
100 gramos |
11.5 |
|
Carne de res (cocida, asada) |
100 gramos |
8.1 |
|
Salmon (cocido, al horno) |
100 gramos |
2.8 |
|
Leche (descremada) |
250 ml |
1.0 |
|
Pavo (cocido, asado) |
100 gramos |
0.9 |
|
Brie (queso) |
100 gramos |
1,8 |
|
Huevo (escalfado) |
1 grande |
0.4 |
|
Pollo (cocido, asado) |
100 gramos |
0.4 |
Tratamiento
de la deficiencia de vitamina B12
Se ha establecido que el
requerimiento diario de vitamina B12 es 2,4 μg/día, pero las cantidades
mayores— 4 a 7 μg/día—las cuales son comunes en las personas que comen carne o
toman un multivitamínico diario, se asocian con valores más bajos de ácido metilmalónico.
El Food and Nutrition Board recomienda que los adultos mayores sanos reciban un
suplemento de vitamina B12 cristalina. Sin embargo, la mayoría de los
pacientes con deficiencia de vitamina B12 tiene malabsorción y requerirán el
reemplazo parenteral u oral en altas dosis. La adecuada suplementación resuelve
la anemia megaloblástica, y resuelve o mejora la mielopatía.
Vitamina
B12 inyectable
Existen muchos regímenes
recomendados para inyectar la vitamina B12 (usualmente cianocobalamina en EE.
UU. e hidroxicobalamina en Europa). Se retiene casi el 10% de las dosis
inyectadas (100 de 1.000 μg). Los pacientes con anormalidades graves deben
recibir inyecciones de 1.000 μg, por lo menos varias veces por semana durante
1-2 semanas, y luego semanalmente hasta obtener una mejoría evidente, para
seguir con inyecciones mensuales. La respuesta hematológica es rápida, con un
aumento a la semana del recuento de reticulocitos y la corrección de la anemia
megaloblástica entre las 6 a las 8 semanas desde el inicio del tratamiento.
Los
pacientes con anemia grave y síntomas cardíacos deben ser tratados con
transfusiones y diuréticos, monitoreando los electrolitos. Los síntomas
neurológicos pueden empeorar transitoriamente y luego disminuir en semanas o
meses. La gravedad y la duración de las anormalidades neurológicas antes del
tratamiento influyen en el grado de recuperación. El tratamiento de la anemia
perniciosa es para toda la vida. Cuando después de la recuperación clínica se
interrumpe la suplementación con vitamina B12, los síntomas neurológicos
recurren dentro de un corto período (unos 6 meses), y la anemia megaloblástica
lo hace en varios años.
Tratamiento oral en altas dosis
El tratamiento oral en altas dosis es efectivo y cada vez más
difundido. Un estudio realizado 45 años atrás mostró que el 0,5 al 4% de la
vitamina B12 marcada con radioactividad puede ser absorbida por difusión pasiva
(sin la intervención del factor intrínseco) tanto por los controles normales
como por los pacientes con anemia perniciosa. Por lo tanto, la dosis oral de
1.000 µg libera de 5 a 40 µg, aun si es ingerida con alimentos.
Un
estudio aleatorizado que comparó una dosis oral de 2.000 µg diarios con el
tratamiento parenteral (7 inyecciones de 1.000 µg de cianocobalamina durante un
período de 1 mes, seguido de inyecciones mensuales) en pacientes con anemia
perniciosa, gastritis atrófica o antecedente de resección ileal, mostró
reducciones similares del volumen corpuscular medio y un aumento del
hematocrito a los 4 meses, en ambos grupos.
Después
del tratamiento, todos los pacientes (4 en cada grupo) con parestesias, ataxia
o pérdida de memoria experimentaron la resolución sintomática o la mejoría. Sin
embargo, los niveles de ácido metilmalónico después del tratamiento fueron
significativamente inferiores con el tratamiento oral diario (169 nmol/l con
tratamiento oral vs. 265 nmol/l con tratamiento parenteral) y los niveles de
vitamina B12 fueron significativamente superiores (1.005 pg/l vs. 325 pg/ml
[741,5 vs. 239.8 pmol/l]). Un trabajo más reciente con un diseño similar y una
preparación de vitamina B12 oral apropiada también mostró niveles
significativamente inferiores de ácido metilmalónico en el grupo con
tratamiento oral, a los 3 meses del seguimiento.
En
un trabajo aleatorizado que comparó los resultados del tratamiento con vitamina
B12 oral (1.000 µg/día, 10 días, seguido de tratamiento semanal durante 4
semanas y luego mensual) con los resultados del tratamiento intramuscular,
comprobó que los 2 grupos tuvieron mejorías similares de las alteraciones
hematológicas y de los niveles de vitamina B12 a los 90 días.
De
una dosis de 3, 10, 40 y 1000 µg de B12 que se administren de forma
intramuscular, se almacenarán en el organismo un 100, 97, 93 y 15%
respectivamente. Si se administraran mensualmente 1.000 µg de forma
intramuscular, los 150 µg retenidos permanecerían un mes en el organismo. A
diferencia de esto, se ha demostrado que de una toma de 10, 50, 500 y 1.000 µg
vía oral se absorben entre el 16, 3, 2 y 1,3%.
Faltan
datos de estudios a largo plazo para evaluar si el tratamiento oral es efectivo
cuando las dosis se administran a intervalos mayores a 1 día. Los estudios en
adultos mayores, muchos de los cuales tenían gastritis atrófica crónica,
mostraron que para corregir los niveles elevados de ácido metilmalónico, el 60%
requirió dosis orales elevadas de vitamina (>500 µg/día).
Los
profesionales que prefieren el tratamiento parenteral sostienen que el
cumplimiento y el monitoreo de los pacientes es mejor debido a su frecuente
contacto con los prestadores de la salud, mientras que los que prefieren la
terapia oral afirman que el cumplimiento es mejor porque los pacientes
consideran que dicho tratamiento es más conveniente, más cómodo y más barato.
Adultos
mayores (>50 años)
Debido
a que la malabsorción y la deficiencia de vitamina B12 son más
comunes en adultos mayores, se recomienda que los adultos mayores de 50 años
tomen entre 100 a 500 μg/día de vitamina B12 suplementaria.
Prevención de Enfermedades
Homocisteína
y enfermedades cardiovasculares
Los estudios epidemiológicos indican que incluso niveles de homocisteína
moderadamente elevados en la sangre incrementan el riesgo de padecer enfermedades cardiovasculares (ECV), aunque el mecanismo por el
cual la homocisteína puede incrementar el riesgo de ECV sigue siendo objeto de una
gran cantidad de investigación. La cantidad de homocisteína en la sangre es
regulada por al menos tres vitaminas: folato, vitamina B6, y vitamina B12 .
El análisis temprano de los resultados de 12 pruebas aleatorias controladas en
la reducción de la homocisteína mostró que la suplementación con ácido fólico
(0.5-5 mg/día) tuvo el mayor efecto reductor sobre los niveles de homocisteína
sanguínea (reducción del 25%); la co-suplementación con ácido fólico y vitamina
B12 (500 μg/día) proporcionó una reducción adicional del 7% (reducción del 32%)
en las concentraciones de homocisteína sanguínea. Se piensa que la elevación de
los niveles de homocisteína podría ser en parte debido a la deficiencia de
vitamina B12 en individuos mayores de 60 años de edad. Dos estudios encontraron
que los niveles sanguíneos de AMM estaban aumentados en más del 60% de los
individuos de edad avanzada con niveles de homocisteína elevados. En la
ausencia de una insuficiencia renal, un nivel elevado de AMM en conjunto con
niveles de homocisteína elevados, indican tanto una deficiencia de vitamina B12
como una deficiencia combinada de vitamina B12 y folato. De tal manera, parece
importante evaluar el estado de la vitamina B12, como también la función renal,
en adultos de edad avanzada con elevados niveles de homocisteína antes de
iniciar una terapia de disminución de la homocisteína.
Estudios de
intervención:
Aunque un
incremento en la ingesta de ácido fólico y vitamina B12 es efectivo en la
disminución de los niveles de homocisteína,
la intervención combinada de estas vitaminas B (ácido fólico y B12) no
disminuyeron el riesgo de ECV. Varias pruebas aleatorias controladas con placebo han sido conducidas a determinar si la disminución de la homocisteína a través
de la suplementación con ácido fólico, vitamina B12, y vitamina B6 reduce la
incidencia de ECV. Un meta análisis de la información de 11 ensayos que incluyeron 45,000 participantes en riesgo
de ECV, mostró que la suplementación de vitaminas B no tuvo algún efecto
significante en el riesgo de infarto de miocardio o accidente cerebrovascular como tampoco modifico el riesgo de
mortalidad por todas las causas. Otros meta-análisis que incluyeron pacientes
con enfermedad renal crónica han confirmado la falta de efecto de la
disminución de la homocisteína en el riesgo de un infarto agudo al miocardio y
muerte. Sin embargo, el riesgo de un accidente cerebrovascular (ACV) fue
reducido de manera significativa en un 7%-12% con la suplementación de vitaminas
del grupo B. Otro meta-análisis de 12 ensayos clínicos
que midieron la vasodilatación mediada por flujo (VMF), que es un marcador sustituto de la salud vascular, en
respuesta a la reducción de la homocisteína reveló que la suplementación de
vitamina B estuvo acompañada por un mejoramiento en la VMF a corto plazo <8
semanas. Además, la alta prevalencia de los desórdenes de mala absorción y la deficiencia de vitamina B12 en
individuos de edad avanzada podrían justificar el uso de dosis más altas de
vitamina B12 que aquellas usadas en estos ensayos; en casos de malabsorción,
solo una terapia de altas dosis orales o inyecciones intramusculares pueden
superar la deficiencia de vitamina B12.
Cáncer
El folato es requerido para la síntesis
del ADN,
y existe evidencia que de que la disponibilidad disminuida de folato resulta en
hebras de ADN que son más susceptibles a dañarse. La deficiencia de vitamina
B12 atrapa el folato en una forma que es inutilizable para el cuerpo en la
síntesis del ADN. Tanto la deficiencia de vitamina B12 como la deficiencia de
folato derivan en una capacidad disminuida para las reacciones de metilación.
De esta manera, la deficiencia de vitamina B12 puede conducir a una tasa de
daño elevada del ADN y a una metilación alterada del ADN, los cuales son
factores importantes del riesgo de padecer cáncer.
Una serie de estudios en adultos jóvenes y adultos mayores señaló que los
niveles incrementados de homocisteína
y los niveles disminuidos de vitamina B12 en la sangre fueron asociados con un biomarcador
de la ruptura de cromosomas en leucocitos. En un estudio doble ciego controlado con placebo,
el mismo marcador de ruptura de cromosomas fue minimizado en adultos jóvenes
que fueron suplementados con 700 μg de ácido fólico y 7 μg de vitamina B12
diariamente a través de cereal, por dos meses.
Un estudio de caso y control comparó los niveles pre diagnósticos
del folato, vitamina B6,
y vitamina B12 en
el suero en 195 mujeres, posteriormente diagnosticadas con cáncer
de mama y de 195 mujeres de edades similares a las cuales no se les diagnosticó
cáncer de mama. Entre las mujeres postmenopáusicas, la asociación entre los
niveles sanguíneos de vitamina B12 y el cáncer de mama mostró un efecto umbral.
El riesgo de cáncer de mama fue más del doble en mujeres con los niveles de
vitamina B12 en el suero en el quintil
más bajo comparado con el de las mujeres en los cuatro quintiles más altos. Sin
embargo, un meta-análisis de siete estudios de casos y controles y siete
estudios de cohorte prospectivos concluyeron que el riesgo de cáncer de seno no
se modificó por ingestas altas versus ingestas bajas de vitamina B12. Se
necesitan más estudios para hacer recomendaciones al respecto.
Defectos del tubo neural
Los defectos del tubo neural (DTN) pueden resultar en anencefalia o espina bífida,
los cuales son malformaciones congénitas mayormente fatales del sistema nervioso central. Los defectos surgen a partir del fracaso del cierre del
tubo neural embrionario, que ocurre entre el 21er. y el 28vo. día después de la
concepción, que es la etapa cuando muchas mujeres son inconscientes de su
embarazo. Pruebas aleatorias controladas han demostrado una reducción del 60%
al100% en casos de DTN cuando las mujeres consumieron suplementos de ácido
fólico en grandes dosis (1 a 5 mg diarios) en adición a una dieta variada
durante el mes anterior y el mes posterior después de la concepción. No se
conocen las causas de esta afección aunque está claro que el ácido fólico no
actúa corrigiendo una deficiencia nutricional. Un defecto metabólico parece ser
el responsable de los DTN. Existe evidencia que indica que el efecto reductor
del ácido fólico sobre la concentración de la homocisteína juega
un papel crítico en la reducción del riesgo de DTN. La homocisteína puede
acumularse en la sangre cuando el folato y/o la vitamina B12 son inadecuados
para el funcionamiento eficaz de la enzima metionina sintasa. Niveles de vitamina B12 disminuidos y concentraciones
elevadas de homocisteína han sido encontrados en la sangre y el líquido
amniótico en mujeres embarazadas en alto riesgo de DTN. El reciente meta-análisis de 12 estudios de casos y controles que incluyó 567 madres con un embarazo
actual o anterior afectado por DTN y 1566 madres que no fueron afectadas,
mostro que un bajo nivel de vitamina B12 materno estuvo asociado con un riesgo
incrementado del riesgo de DTN. Sin embargo aún no se ha evaluado si la
suplementación de vitamina B12 puede ser beneficiosa en la prevención de DTN.
Deterioro
cognitivo, demencia, y enfermedad de Alzheimer
La ocurrencia
de la deficiencia de vitamina B12 prevalece en la población de edad avanzada y
ha sido frecuentemente asociada con la enfermedad de Alzheimer. Un estudio encontró niveles más bajos de vitamina B12
en el líquido cefalorraquídeo en pacientes con Alzheimer que en pacientes con otros
tipos de demencia,
aunque los niveles sanguíneos de vitamina B12 no difirieron. La razón para la
asociación de un bajo estatus de vitamina B12 con la enfermedad de Alzheimer aún
no está clara. La deficiencia de vitamina B12, al igual que la deficiencia de folato,
puede conducir a una disminución de la síntesis de metionina y S-adenosil metionina (SAM), de este modo afecta adversamente las reacciones
de metilación.
Las reacciones de metilación son esenciales para el metabolismo de los componentes de la vaina de mielina de las células nerviosas así como de los neurotransmisores.
Otras implicaciones metabólicas de la deficiencia de vitamina B12 incluyen la
acumulación de la homocisteína y el ácido metilmalónico, que podría contribuir
a las características neuropatológicas de la demencia. El advenimiento de test
diagnósticos más adecuados, incluyendo los ensayos para homocisteína y AMM, ha
revelado una prevalencia sorprendentemente alta de una forma más sutil de
deficiencia subclínica de B12, particularmente entre los adultos mayores. Esto
a menudo se asocia con desmejoramiento cognitivo y demencia, incluyendo
enfermedad de Alzheimer.
También se ha reportado deficiencia de B12 en asociación con otros desórdenes neurodegenerativos
incluyendo demencia vascular, enfermedad de Parkinson y esclerosis múltiple. Estas
condiciones están todas asociadas con neuro-inflamación crónica y estrés
oxidativo. Es posible que estas asociaciones clínicas reflejan un metabolismo
de la vitamina B12 comprometido debido a tal estrés. Por su parte se ve una considerable
variación inter-individual en la respuesta clínica a la terapia de reemplazo
con vitamina B12. Se necesitan más estudios para determinar hasta cuanto esto es atribuible a
determinantes genéticos de la absorción, la distribución y la captación celular
de la vitamina B12.
Una gran
mayoría de estudios transversales (en estos estudios las variables se observan durante un
determinado punto del tiempo) y de cohorte prospectivos (en estos estudios se definen o clasifican a los
participantes por la presencia o ausencia de una determinada característica o
exposición y se los estudia hacia adelante en el tiempo comparando entre ambos
grupos la frecuencia de aparición de la variable en estudio) han asociado elevadas concentraciones de homocisteína con mediciones de resultados cognitivos pobres y un riesgo incrementado de demencia,
incluyendo la enfermedad de Alzheimer. Un estudio de caso y control en 164 pacientes con demencia del
tipo de Alzheimer incluyó 76 casos en los que se confirmó el diagnóstico de la
enfermedad de Alzheimer al examinarse las células cerebrales después de su
muerte. Comparados con los 108 sujetos de control sin evidencia de demencia,
los sujetos con demencia del tipo Alzheimer y con enfermedad de Alzheimer
confirmada tuvieron niveles sanguíneos de homocisteína más altos y niveles
sanguíneos de folato y vitamina B12 más bajos. Las mediciones del estado
nutricional general señaló que la asociación de los niveles de homocisteína
aumentados y un estado de vitamina B12 disminuido junto a la enfermedad de
Alzheimer no se debió a una malnutrición relacionada a la demencia. En una
muestra de 1,092 hombres y mujeres sin demencia con un seguimiento por un
promedio de 10 años, aquellos con niveles más altos de homocisteína en el
plasma al inicio del estudio tuvieron un riesgo significativamente más alto de
desarrollar la enfermedad de Alzheimer y otros tipos de demencia.
Específicamente, aquellos con niveles de homocisteína plasmática mayores a 14
μmol/L tuvieron un riesgo casi doble de desarrollar la enfermedad de Alzheimer.
Un estudio en 650 hombres y mujeres ancianos reportó que el riesgo de niveles
elevados de homocisteína plasmática fue significativamente más elevado en
aquellos con resultados más bajos de la función cognitiva. Un estudio
prospectivo en 816 hombres y mujeres ancianos reportó que aquellos con hiperhomocisteinemia (niveles de homocisteína >15 μmol/L) tuvieron un
riesgo significativamente más alto de desarrollar enfermedad de Alzheimer o
demencia. Una reciente revisión sistemática de 35 estudios de cohorte prospectivo que evaluaron la
asociación ente el estatus de la vitamina B12 y el deterioro cognitivo en
individuos mayores con o sin demencia al inicio del estudio no apoyo una relación
entre las concentraciones de vitamina B12 en el suero y una disminución
cognitiva, demencia o enfermedad de Alzheimer. No obstante, estudios que
utilizaron biomarcadores más sensibles del estatus de la vitamina B12, incluyendo mediciones de la holo-transcobalamina, y el AMM
mostraron resultados más consistentes y una tendencia hacia la asociación entre
un estado pobre de la vitamina B12 y una disminución cognitiva más rápida y el
riesgo de la enfermedad de Alzheimer.
Estudios de
intervención:
Una
suplementación de altas dosis de vitaminas del grupo B ha probado su
efectividad al tratar la hiperhomocisteinemia en individuos de edad avanzada con o sin un deterioro cognitivo.
Un ensayo clínico aleatorio doble ciego controlado con placebo en 900 individuos de mayor edad en un riesgo alto de deterioro
cognitivo encontró que la suplementación diaria de 400 μg de ácido fólico y 100
μg de vitamina B12 por dos años mejoro significativamente las medidas de
memoria inmediata y retardada. Otro estudio aleatorio controlado con placebo de
un lapso de 2 años en adultos ancianos reporto que un régimen diario de 800 μg
de ácido fólico, 500 μg de vitamina B12 y 20 mg de vitamina B6, redujo
significantemente la tasa de atrofia cerebral comparado con el tratamiento con placebo (0.5% vs. 3.7%).
Curiosamente, un beneficio mayor fue observado en aquellos pacientes con alta concentración
de homocisteína en comparación con baja concentración de homocisteína al inicio
del estudio, sugiriendo la importancia de la disminución de los niveles de
homocisteína en la prevención de atrofia cerebral y el deterioro cognitivo. Los
autores atribuyeron los cambios en los niveles de homocisteína ante todo a la
vitamina B12. Finalmente el ensayo clínico más reciente, aleatorio, doble
ciego, controlado con placebo, realizado en aproximadamente 2,500 individuos
que sufrieron un accidente cerebrovascular mostró que la normalización de las
concentraciones de homocisteína debido a la suplementación de vitaminas del
grupo B (2 mg de ácido fólico, 500 μg de vitamina B12, y 25 mg de vitamina B6)
no mejoró el rendimiento cognitivo ni disminuyó la incidencia de un deterioro
cognitivo en comparación con el placebo. Actualmente, hay una necesidad de
ensayos más amplios para evaluar el efecto de la suplementación de vitaminas
del grupo B en los resultados a largo plazo, como lo es la incidencia de la enfermedad de Alzheimer (EA), pero se ha visto que el tratamiento con estas vitaminas
puede reducir la atrofia de materia gris en regiones específicamente
vulnerables al proceso de la EA, como el lóbulo temporal medial, el cual
incluye estructuras como el hipocampo y la corteza perirrinal entre otras.
Estas estructuras y su relación con la corteza cerebral se relacionan con la
memoria y su atrofia se relaciona con el deterioro cognitivo.
En el último
meta análisis realizado para evaluar la eficacia de la suplementación con ácido
fólico y vitamina B12 en pacientes con deterioro cognitivo leve y en ancianos
sin deterioro cognitivo se estudiaron un total de 21 ensayos controlados y
aleatorizados que involucraron a 7571 participantes. Los autores concluyen que
la suplementación puede demorar el deterioro cognitivo en ancianos y
recomiendan que los suplementos de vitaminas B (especialmente ácido fólico y
B12) deberían considerarse como una medicación preventiva en pacientes con deterioro
cognitivo leve o en adultos mayores sin deterioro cognitivo.
Estudios observacionales han encontrado que hasta el 30% de los pacientes hospitalizados
por depresión son deficientes en vitamina B12. Un estudio transversal de 700 mujeres físicamente discapacitadas que viven en
comunidad con una edad por encima de los 65 años, encontró que las mujeres
deficientes de vitamina B12 eran dos veces más propensas a estar severamente
deprimidas que las mujeres sin deficiencia. Un estudio de base poblacional en
3,884 hombres y mujeres ancianos con trastornos depresivos encontró que
aquellos con una deficiencia de vitamina B12 eran casi 70% más propensos a
sufrir de depresión que aquellos con un estatus normal de vitamina B12. Las causas de la relación entre la deficiencia de
vitamina B12 y la depresión no son claras, pero podrían involucrar una escasez
de S-adenosilmetionina (SAM). La SAM es un donante del grupo metilo en
numerosas reacciones de metilación en el cerebro, incluyendo aquellas involucradas en el metabolismo de los neurotransmisores cuya deficiencia ha sido relacionada con la depresión. Una deficiencia severa
de B12 en un modelo de ratón mostró alteraciones notables en la metilación al
nivel del ADN en el cerebro, que podrían conducir a alteraciones neurológicas.
Esta hipótesis se sostiene en varios estudios que han demostrado que la
suplementación con SAM mejora los síntomas depresivos.
El nivel aumentado
de homocisteína es otro biomarcador no específico de la deficiencia de vitamina B12 que ha sido ligado a síntomas
depresivos en los ancianos. Algunos pocos estudios han examinado la relación
del estatus de la vitamina B12, los niveles de homocisteína y el desarrollo de
la depresión con el tiempo. En un estudio de intervención aleatorio controlado con placebo en un poco más de 900 participantes mayores que experimentaron malestar
psicológico, una suplementación con ácido fólico (400 μg) y vitamina B12 (100
μg) por dos años no redujo la ocurrencia de síntomas de depresión a pesar de la
mejora significativa de los niveles de folato, vitamina B12 y homocisteína en
la sangre a comparación con el placebo. Sin embargo, en un estudio a largo
plazo, aleatorio, doble ciego,
controlado con placebo entre enfermos con accidentes cerebrovasculares en un
riesgo alto de depresión, suplementados diariamente con 2 mg de ácido fólico,
25 mg de vitamina B6 y 500 μg de vitamina B12 se redujo significativamente el
riesgo de mayores episodios depresivos durante un periodo de seguimiento de
siete años comparado con el placebo. Aunque aún no puede ser determinado si la
deficiencia de vitamina B12 juega un papel causal en la depresión, podría ser
beneficioso cubrir la deficiencia de vitamina B12 en individuos de edad
avanzada como parte de una evaluación médica para la depresión.
Niveles altos
de homocisteína podrían afectar la remodelación ósea al incrementar la resorción ósea,
disminuyendo la formación ósea, y reduciendo el flujo sanguíneo óseo. Otro
mecanismo propuesto involucra la unión de la homocisteína a la matriz de colágeno del hueso, la cual puede modificar las propiedades del colágeno y reducir la resistencia ósea. Las alteraciones de las propiedades biomecánicas
del hueso pueden contribuir a la osteoporosis e incrementar el riesgo de fracturas en los ancianos. Debido a que la vitamina B12 es un determinante del
metabolismo de la homocisteína, se sugirió que el riesgo de fracturas
osteoporóticas en sujetos de mayor edad podrían ser más ocurrentes por una
deficiencia de vitamina B12. Un meta-ánalisis
de cuatro estudios observacionales que dieron seguimiento de 3 a 16 años a un total de
7,475 individuos de mayor edad, encontró una débil asociación entre una
elevación en la vitamina B12 de 50 picomoles/L en la sangre y una reducción en
el riesgo de fracturas. Un ensayo aleatorio controlado con placebo en 559 individuos ancianos con bajos niveles de folato y vitamina B12 en el suero y un riesgo incrementado del riesgo de fracturas evaluó la suplementación
combinada de muy altas dosis de ácido fólico (5 mg/día) y vitamina B12 (1.5
mg/día). El estudio de dos años encontró que la suplementación mejoro el
estatus de la vitamina B, disminuyó las concentraciones de homocisteína, y
redujo el riesgo de fracturas totales en comparación con el placebo. Sin
embargo un estudio multicéntrico en 5,485 sujetos con enfermedades cardiovasculares o diabetes mellitus mostró que la suplementación diaria de ácido fólico (2.5 mg), vitamina B12
(1mg) y vitamina B6 (50 mg) disminuyó las concentraciones de homocisteína pero
no tuvo efecto en el riesgo de fracturas en comparación con el placebo. Hacen
falta más estudios para definir la utilidad de la suplementación de vitamina
B12 en el tratamiento de la osteoporosis.
Toxicidad
Efectos
tóxicos o adversos no han sido asociados con grandes ingestas de vitamina B12
proveniente de alimentos o de suplementos en personas sanas. Se han utilizado
dosis orales de hasta 2 mg (2,000 μg) diariamente o de 1 mg al mes por
inyección intramuscular (IM) para tratar la anemia perniciosa sin efectos
secundarios significativos. Cuando se administran oralmente altas dosis de
vitamina B12, sólo un pequeño porcentaje puede ser absorbido, lo que
podría explicar la baja toxicidad. Debido a la baja toxicidad de la vitamina B12,
ningún nivel máximo de ingesta tolerable ha sido establecido por la Junta de
Nutrición y Alimentos Estadounidense.
Interacción
con fármacos
Una serie de
drogas reducen la absorción de la vitamina B12. Los inhibidores de
la bomba de protones (por ejemplo, omeprazol y lansoprazol), usados en la
terapia del síndrome de Zollinger-Ellison y del reflujo gastroesofágico, reducen
notablemente la secreción de ácido estomacal requerida para la liberación de la
vitamina B12 de los alimentos, aunque no de la de los suplementos.
Se ha encontrado que la utilización a largo plazo de inhibidores de la bomba de
protones disminuye los niveles sanguíneos de vitamina B12. Sin
embargo, la deficiencia de vitamina B12 generalmente no se
desarrolla hasta por lo menos después de tres años de terapia continua. Otra
clase de inhibidores de la producción de ácido gástrico conocidos como
antagonistas de los receptores de histamina 2 (receptor-H2), entre ellos
cimetidina, famotidina, y ranitidina, también disminuyen la absorción de
vitamina B12 de los alimentos. No está claro si el uso a largo plazo
de los antagonistas de los receptores-H2 podrían causar una deficiencia evidente
de vitamina B12. Los individuos que toman fármacos que inhiben la
secreción de ácido gástrico deberían considerar tomar vitamina B12
en forma de suplementos porque el ácido gástrico no es requerido para su
absorción. Otras drogas que se han encontrado que inhiben la absorción de
vitamina B12 de los alimentos incluyen colestiramina (una resina que
se une a los ácidos biliares utilizada en el tratamiento del colesterol
elevado), cloramfenicol y neomicina (antibióticos), y colchicina (medicamento usado
en el tratamiento de la gota). La
colchicina induce
malabsorción reversible de B12 por reducción de los receptores para el factor
intrínseco en la mucosa intestinal La
metformina, un medicamento ampliamente usado para el tratamiento de la diabetes
tipo 2 (se estima que unos 100 millones de personas usan este medicamento en
todo el mundo), disminuye la absorción de vitamina B12 a través de
la ligadura del calcio libre necesario para la absorción del complejo FI-B12 .
Sin embargo, el significado clínico de esto no está claro. No se conoce si la
suplementación con calcio puede revertir la malabsorción de vitamina B12;
por ello, la suplementación con calcio no está actualmente prescrita para la
prevención o tratamiento de la deficiencia de vitamina B12 inducida
por la metformina. Reportes previos de que megadosis de vitamina C destruyan la
vitamina B12 no han sido comprobados y podrían haber sido un
artefacto del ensayo utilizado para medir los niveles de vitamina B12.
Grandes dosis
de ácido fólico administradas a un individuo con una deficiencia de vitamina B12
no diagnosticada podría corregir la anemia megaloblástica sin corregir la
deficiencia de vitamina B12 subyacente, dejando a la persona en
riesgo de sufrir daño neurológico irreversible. Por esta razón la Junta de
Nutrición y Alimentos del Instituto de Medicina Estadounidense aconseja que
todos los adultos limiten su ingesta de ácido fólico (suplementos y alimentos
fortificados) a 1,000 μg (1 mg) diarios.
Estudios
recientes sugieren que la coincidencia de niveles suprafisiológicos de folato
sérico con déficit de B12 aumentan el deterioro cognitivo y la anemia. También
se observó aumento en las concentraciones plasmáticas de homocisteína total y
de ácido metilmalónico (dos indicadores funcionales del estado de B12), con
aumento de folato plasmático en estados de baja B12. Estos datos implican
fuertemente que la elevación plasmática de folato está asociado con la
exacerbación del estado bioquímico y clínico de la deficiencia de B12.
Hay consenso
internacional sobre la necesidad de asegurar un adecuado aporte de B12, en
especial a los adultos mayores, en caso de fortificación con ácido fólico.
Consideraciones
finales
Una dieta
variada debería proporcionar suficiente vitamina B12 como para
prevenir una deficiencia en la mayoría de los individuos de 50 años de edad o
menos. Los vegetarianos estrictos y las mujeres que planean embarazarse deben
tomar diariamente un suplemento multivitamínico que pueda asegurar una ingesta
de 6 a 30 μg de vitamina B12 de una forma que sea fácilmente
absorbida. Los suplementos de dosis más altas de vitamina B12 son
recomendados a pacientes que ya presentan una deficiencia o que toman
medicamentos que interfieren con su absorción.
Glosario:
Anemia macrocítica: Conteo bajo de glóbulos
rojos, caracterizado por la presencia en la sangre de glóbulos rojos más
grandes de los normal.
Aplasia medular: La aplasia medular es una
enfermedad en la que la médula ósea roja desaparece y por tanto se deja de
producir glóbulos rojos, glóbulos blancos y plaquetas. Puede ser congénita o
adquirida.
Ataxia: Falta de coordinación o inestabilidad usualmente relacionada a una
alteración en el cerebelo, una parte del sistema nervioso central que regula la
coordinación y el equilibrio.
Cohorte: Grupo de personas seguidas a través
del tiempo como parte de un estudio epidemiológico.
Ensayo controlado aleatorio/aleatorizado (ECA): Ensayo clínico con al menos un grupo
de tratamiento activo y un grupo control (placebo). En los ECA, los
participantes son elegidos para los grupos experimental y de control de forma
aleatoria y no se les dice si están recibiendo el tratamiento activo o el
placebo hasta el final del estudio. Este tipo de diseño de estudio puede
aportar evidencia de causalidad.
Ensayo cruzado: Ensayo clínico donde se aplican dos intervenciones o dos tratamientos a
los mismos individuos después de un periodo de limpieza apropiado. Uno de los
tratamientos a menudo es un placebo. En un diseño cruzado aleatorizado, las
intervenciones se aplican en orden aleatorio para asegurar que el orden de los
tratamientos no contribuya al resultado.
Ensayo de intervención: Estudio experimental (usualmente un ensayo clínico) utilizado para
probar el efecto de un tratamiento o intervención sobre resultados relacionados
con salud o enfermedad.
Enterocitos: Células que componen la superficie luminal (interna) del intestino.
Estudio
de caso y control: Estudio en
el que la exposición de las personas que han sido diagnosticadas con una
enfermedad (casos) se compara con el de las personas sin la enfermedad
(controles). Los resultados de los estudios de caso y control son más propensos
a ser distorsionados por sesgos en la selección de los casos y controles (sesgo
de selección) y en el recuerdo de la dieta (sesgo de memoria) que los estudios
de cohorte prospectivos.
Estudio
de cohorte: Estudio que
sigue a un gran número de personas por un largo periodo de tiempo, con
frecuencia 10 años o más. En los estudios de cohorte, la información dietética
se reúne antes de que aparezca la enfermedad, en vez de depender de lo
recopilado después de que la enfermedad se desarrolla.
Estudio
de cohorte prospectivo: Estudio basado en la observación en el que se entrevista o
examina a un grupo de personas—conocido como cohorte—en busca de factores de riesgo,
y luego se les controla en oportunidades posteriores para determinar su estado
respecto a los resultados de salud o enfermedad.
Estudio
de corte transversal: Estudio de un grupo de personas en un momento determinado para estudiar
si una exposición se encuentra asociada con la ocurrencia de una enfermedad.
Debido a que el resultado de la enfermedad y la exposición (por ej., la ingesta
de nutrientes) se registran al mismo tiempo, un estudio de corte transversal
aporta una "visión fotográfica" de su relación. Un estudio de corte
transversal no puede aportar información acerca de la causalidad.
fL:(Femtolitro): Unidad de volumen en el
Sistema Internacional de Unidades, equivalente a la milbillonésima parte de un
litro, ó 10-15 litros.
Hematocrito: Porcentaje de glóbulos
rojos en el total de la sangre.
Leucopenia: Disminución de los
glóbulos blancos
Megaloblastosis: Presencia en la sangre de células nucleadas, inmaduras y de gran tamaño
(megaloblastos) que son las precursoras de los glóbulos rojos. Los glóbulos
rojos maduros no tienen núcleo.
Meta Análisis: Técnica estadística
usada para combinar los resultados de diferentes estudios para obtener un
estimado cuantitativo del efecto general de una intervención o exposición
particular sobre un resultado definido.
Microcitosis: Presencia en la sangre
de glóbulos rojos de tamaño menor al normal.
Movimientos mioclónicos: Son movimientos
musculares rápidos, repentinos, breves e involuntarios, de intensidad y frecuencia
variables.
Neutrófilos: Los neutrófilos son un
tipo de glóbulos blancos que actúan en la defensa e inmunidad del organismo.
Representan el porcentaje más alto de los glóbulos blancos en el torrente
sanguíneo y se clasifican en neutrófilos segmentados y neutrófilos en banda.
Estos últimos se crean y almacenan en la médula ósea y se liberan a la sangre
cuando están maduros, pasando a llamarse neutrófilos segmentados o
polimorfonucleares, debido a que son glóbulos blancos que poseen dos o más
lóbulos en su núcleo, es decir con un núcleo multilobulado que se ve como
segmentado.
Neutrófilos hipersegmentados: La hipersegmentación
nuclear es una anomalía de los neutrófilos cuando presentan más de 5 lóbulos en
su núcleo. Su presencia se asocia fuertemente con anemia megaloblástica
(deficiencia de vitamina B12 y/o ácido fólico)
pero también pueden encontrarse en otras patologías como ser infecciones
crónicas, trastornos mieloproliferativos, deficiencia de hierro y por el uso de
algunos fármacos, entre otras causas posibles.
Pancitopenia: Disminución de los tres
tipos de células sanguíneas (glóbulos rojos, glóbulos blancos y plaquetas).
Parestesia: Trastorno de la
sensibilidad de tipo irritativo que se manifiesta con sensaciones anormales sin
estímulo previo, como el hormigueo o el adormecimiento. Esta sensación suele
darse en los brazos, manos, dedos, piernas y pies, aunque puede ocurrir en
cualquier parte del cuerpo.
Picomoles: el mol es una unidad de
medida que expresa cantidad de sustancia, muy utilizada en química y en
estudios médicos. Pico es un prefijo usado en el Sistema Internacional de
Medidas que indica un factor de 10-12, o sea que un picomol es la
billonésima parte de un mol. Para convertir pg de B12/ml a pmol de B12/L hay
que multiplicar por 0,7378.
Receptor: Se
denomina receptor a moléculas especializadas que pueden estar en el interior o
en la superficie de las células a los que se unen sustancias específicas
denominadas ligandos. Los ligandos pueden ser endógenos, o sea, producidos por
el propio organismo, por ejemplo una hormona, o exógenos, o sea que ingresan al
organismo desde el exterior de manera intencional o no, como por ejemplo
un medicamento o un tóxico ambiental. Al
unirse los ligandos a los receptores usualmente provocan un cambio en la
actividad celular modulando diversos procesos.
Reticulocitos: Los reticulocitos son
glóbulos rojos que no han alcanzado su total madurez. Se encuentran en
niveles elevados en el plasma sanguíneo por causa de algunas anemias, cuando el
organismo incrementa la producción de glóbulos rojos y los envía al torrente
sanguíneo antes de que sean maduros.
Síndrome de Zollinger-Ellison: Se trata de un tumor
que secreta gastrina, la cual incrementa la producción de ácido gástrico
provocando úlceras graves y recurrentes en el esófago, el estómago, y la
porciones superiores del intestino delgado.
Síndrome Urémico Hemolítico: Es una enfermedad
grave, caracterizada por daño agudo de los riñones, asociado a alteraciones en
las células de la sangre: trombocitopenia (reducción de plaquetas, necesarias
para formar los coágulos) y anemia (causada por ruptura anormal de glóbulos
rojos).
Talasemia: Trastorno hereditario en
el cual los pacientes tienen una producción anormal de glóbulos rojos con
defectos en la formación de hemoglobina.
Trombocitopenia: Disminución de la
cantidad de plaquetas.
Vitiligo: Es una enfermedad
cutánea en la cual hay una pérdida del color (pigmento) de zonas de piel. El
resultado es la aparición de parches (áreas planas de cambio de color en
la piel) blancos y desiguales que no tienen pigmento pero se sienten como
piel normal. Es una enfermedad
autoinmune asociada
frecuentemente a otras enfermedades
autoinmunes, como la anemia perniciosa.
Volumen corpuscular medio: Es el volumen promedio
que ocupa un glóbulo rojo. El valor se expresa en femtolitros (fL) o en
micrones cúbicos µm3.
Bibliografía:
Kozyraki
R, Cases O. Vitamin B12 absorption: mammalian physiology and acquired and
inherited disorders. Biochimie. 2013 May;95(5):1002-7. doi:
10.1016/j.biochi.2012.11.004. Epub 2012 Nov 20. PMID: 23178706.
HEMATOLOGÍA,
Vol 19: 208 - 221 Número Extraordinario XXII CONGRESO Octubre 2015 Alberto
Lazarowski Transporte de vitamina B12 Un laberinto de una única entrada y
múltiples caminos incompletos.
Oregon State
University. Linus Pauling Institute – Centro de Información de micronutrientes.
Sociedad Argentina de Nutrición. Actualización en Nutrición Vol 22. N°3.
2021 | Julio-Septiembre de 2021. Isabel Bianchi di Carcano, Marisa Armeno. Déficit de vitamina B12
en grupos vulnerables con alimentación omnívora
Sally P. Stabler M.D. N Engl J Med 2013;368:149-60. Vitamin B12 Deficiency.
Sukumar N,
Saravanan P. Investigating vitamin B12 deficiency BMJ 2019; 365 :l1865
doi:10.1136/bmj.l1865
Watanabe F,
Yabuta Y, Tanioka Y, Bito T. Biologically active vitamin B12 compounds in foods
for preventing deficiency among vegetarians and elderly subjects. J Agric Food
Chem. 2013;61(28):6769-6775. (PubMed)
Tomohiro Bito, Fei Teng, Noriharu Ohishi, ShigeoTakenaka, Emi Miyamoto, Emi Sakuno, Kazuhisa Terashima, Yukinori Yabuta, Fumio Watanabe.
Characterization of vitamin B12 compounds
in the fruiting bodies of shiitake mushroom (Lentinula edodes) and bed
logs after fruiting of the mushroom. Mycoscience
Volume
55, Issue 6, November 2014, Pages 462-468.
Rizzo,
Gianluca & Laganà, Antonio Simone. A review of vitamin B12 analogues can
block b12 absorption.(2020) 6.p105-129.
Quinlivan EP,
McPartlin J, McNulty H, et al. Importance of both folic acid and vitamin B12 in
reduction of risk of vascular disease. Lancet. 2002;359(9302):227-228. (PubMed)
Rogne T,
Tielemans MJ, Chong MF, etal . Associations of maternal vitamin B12
concentration in pregnancy with the risks of preterm birth and low birth
weight: a systematic review and meta-analysis of individual participant data.
Am J Epidemiol 2017; 185:212-223.
Sukumar N,
Rafnsson SB, Kandala NB, Bhopal R, Yajnik CS, Saravanan P. Prevalence of
vitamin B-12 insufficiency during pregnancy and its effect on offspring birth
weight: a systematic review and meta-analysis. Am J Clin Nutr 2016;
103:1232-51.
Marti-Carvajal
AJ, Sola I, Lathyris D, Karakitsiou DE, Simancas-Racines D.
Homocysteine-lowering interventions for preventing cardiovascular events.
Cochrane Database Syst Rev. 2013;1:CD006612. (PubMed)
Huang T, Chen
Y, Yang B, Yang J, Wahlqvist ML, Li D. Meta-analysis of B vitamin
supplementation on plasma homocysteine, cardiovascular and all-cause mortality.
Clin Nutr. 2012;31(4):448-454. (PubMed)
Ji Y, Tan S,
Xu Y, et al. Vitamin B supplementation, homocysteine levels, and the risk of
cerebrovascular disease: A meta-analysis. Neurology. 2013;81(15):1298-1307.
(PubMed)
Potter K,
Hankey GJ, Green DJ, Eikelboom J, Jamrozik K, Arnolda LF. The effect of
long-term homocysteine-lowering on carotid intima-media thickness and
flow-mediated vasodilation in stroke patients: a randomized controlled trial
and meta-analysis. BMC Cardiovasc Disord. 2008;8:24. (PubMed)
Qin X, Xu M,
Zhang Y, et al. Effect of folic acid supplementation on the progression of
carotid intima-media thickness: a meta-analysis of randomized controlled trials.
Atherosclerosis. 2012;222(2):307-313. (PubMed)
Fenech M.
Folate (vitamin B9) and vitamin B12 and their function in the maintenance of
nuclear and mitochondrial genome integrity. Mutat Res. 2012;733(1-2):21-33.
(PubMed)
Wu
W, Kang S, Zhang D. Association of vitamin B6, vitamin B12 and methionine with
risk of breast cancer: a dose-response meta-analysis. Br J Cancer.
2013;109(7):1926-1944. (PubMed)
McCaddon
A. Vitamin B12 in neurology and ageing; clinical and genetic aspects.
Biochimie. 2013;95(5):1066-1076. (PubMed)
Smith AD,
Smith SM, de Jager CA, et al. Homocysteine-lowering by B vitamins slows the
rate of accelerated brain atrophy in mild cognitive impairment: a randomized
controlled trial. PLoS One. 2010;5(9):e12244. (PubMed)
Douaud G,
Refsum H, de Jager CA, et al. Preventing Alzheimer's disease-related gray
matter atrophy by B-vitamin treatment. Proc Natl Acad Sci U S A.
2013;110(23):9523-9528. (PubMed)
Walker JG,
Mackinnon AJ, Batterham P, et al. Mental health literacy, folic acid and
vitamin B12, and physical activity for the prevention of depression in older
adults: randomised controlled trial. Br J Psychiatry. 2010;197(1):45-54.
Van
Wijngaarden JP, Doets EL, Szczecinska A, et al. Vitamin B12, folate,
homocysteine, and bone health in adults and elderly people: a systematic review
with meta-analyses. J Nutr Metab. 2013;2013:486186. (PubMed)
Food
and Nutrition Board, Institute of Medicine. Vitamin B12. Dietary Reference
Intakes: Thiamin, Riboflavin, Niacin, Vitamin B6, Vitamin B12, Pantothenic Acid,
Biotin, and Choline. Washington D.C.: National Academy Press; 1998:306-356.
(National Academy Press)
Selhub J, Savaria Morris M, Jacques P.F, Rosenberg I.H.
Folate-vitamin B-12 interaction in relation to cognitive impairment, anemia and
biochemical indicators of vitamin B-12 deficiency. J Clin Nutr Febrero de 2009;
89 (2): 702S-6S.
Mazokopakis
EE, Starakis IK. Recommendations for diagnosis and management of
metformin-induced vitamin B12 (Cbl) deficiency. Diabetes Res Clin Pract.
2012;97(3):359-367. (PubMed)
Albai O,
Timar B, Paun DL, Sima A, Roman D, Timar R. Metformin
Treatment: A Potential Cause of Megaloblastic Anemia in Patients with Type 2
Diabetes Mellitus.
Diabetes
Metab Syndr Obes. 2020 Oct 21;13:3873-3878. doi: 10.2147/DMSO.S270393.
eCollection 2020.
Li,
S., Guo, Y., Men, J. et al. The preventive efficacy of vitamin B
supplements on the cognitive decline of elderly adults: a systematic review and
meta-analysis. BMC Geriatr 21, 367 (2021).
Ángel Mejía,
Gilberto. Diccionario de Laboratorio aplicado a la Clínica. 2da. edición –
Editorial Médica Panamericana, 2000.
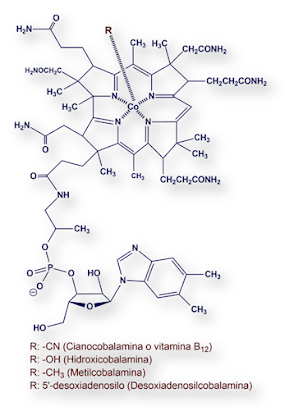



Comentarios
Publicar un comentario